
생화학분자생물학회입니다.
Laboratory of GPCR & Inflammation in the Airway
작성자
관리자작성일자
2017-01-01조회수
625Laboratory of GPCR & Inflammation in the Airway
송경섭
고신대학교 의과대학 생리학교실
[연구실소개]
본 실험실에서는 인간의 호흡기에서 외부의 미세먼지, 미생물, 박테리아, 바이러스에 의해 일차면역시스템인 염증이 일어나는데 이를 G-Protein Coupled Receptor(GPCR) 수준에서 염증억제 물질을 개발하는 연구를 한다. 호흡기 염증은 주로 점액의 과분비(Mucus Hypersecretion)과 과발현/과생성(Overproduction) 되는 특성을 가지고 있어서, 비염, 축농증, 중이염, COPD, Cystic Fibrosis 등을 유발할 수 있다. 본 연구실은 2010년에 만들어져서 지금까지 16편의 SCI 논문을 게재하였는데, 주된 내용은 호흡기 염증을 유발하는 인자에 의한 세포 내 신호전달 체계를 규명하고, 이를 억제할 수 있는 세포 내 조절 단백질이나 펩타이드를 개발하여 호흡기 염증을 최대한 줄일 수 있는 신약후보 물질의 개발이다. 본 실험실에서는 학문간의 경계영역에 대한 새로운 응용주제 도출 및 원리 규명을 해야 하는 작업을 거쳐야 하기에 다양한 공동연구가 필수이며 의약학 연구진들과 정보를 교류하며 실제적으로 인간의 삶을 향상시킬 수 있는 주제들에 대한 학제간(Interdisciplinary) 공동연구를 진행하고 있다.
현재 박테리아에서 나오는 독소물질을 이용하여 항염치료 기전 및 마우스 모델에서 염증 조절 단백질을 규명을 하고 있으며, 미세먼지에 의한 호흡기 질환을 기초와 임상을 연결하는 다음과 같은 내용의 중개연구분야를 수행하고 있다. 또한 산업화의 발달에 따라 증가된 대기오염으로 인한 호흡기 질환의 기전 및 그의 억제 단백질을 개발하고 있다.
[연구내용]
1. 박테리아에 의한 밀착연접단백질의 파괴 및 호흡기 염증 기전 연구
대부분의 호흡기 질환은 외부로부터 유입된 세균, 바이러스와 같은 미생물들이 개방된 호흡기의 점막에 다양한 면역반응을 유발하면서 과도하게 염증이 생겨 발병되는데, 이 질환은 염증을 조절함으로써 치료(또는 예방)할 수 있다. 호흡기에 치명적인 박테리아는 P.aeruginosa, S.aureus, Non-Typable H.influenzae 이 대표적이다. 이 박테리아에 감염 시 호흡기에 치명적인 질환이 유발되며, 특히 P.aeruginosa는 항생제 내성을 가지는 박테리아로 더 크게 역할을 할 것으로 예상하고 있다. 박테리아에 의한 세포 내 침윤기전 및 염증발생을 G-Protein Coupled Receptor/G-Protein 레벨에서 연구하고 있으며, 특히 인간 호흡기(상기도/하기도, 폐)에서는 특이적 GPCR이 발현되고, 다양한 염증원이나 미생물, 대기오염군에 의해 다양한 세포 신호 전달이 이루어진다. 본 연구실에서는 다양한 세포 내 신호 전달 기전을 규명하고, 이를 억제하는 세포 내 단백질 발굴 및 박테리아의 침윤을 억제하기 위해 물질을 개발하고 있다.
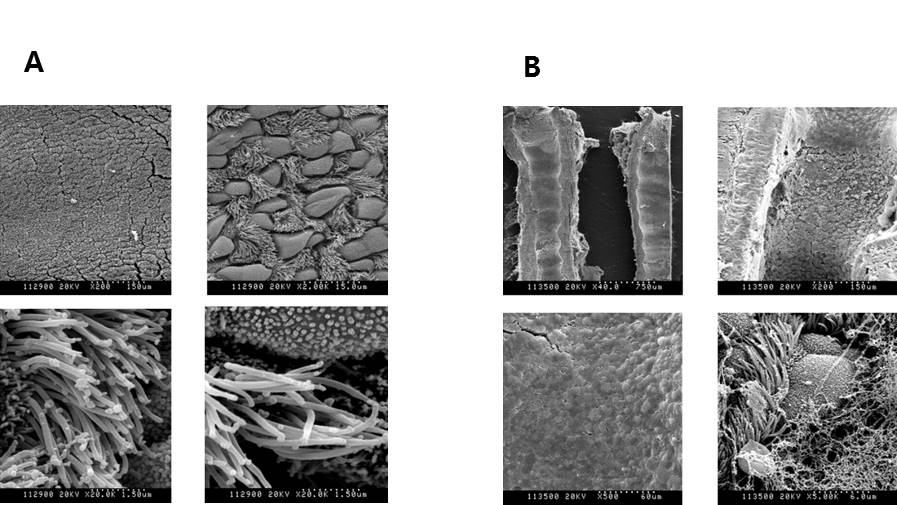
그림 1. 쥐의 호흡기에 박테리아 LPS를 주입 후 기도(Trachea) 전자 현미경사진. (A) Control 마우스의 기도는 술잔세포와 섬모세포들이 선명하게 관찰되어지며 (A, Upper Panel), Cilia 또한 건강하고 선명하게 보여지는 반면, (B) LPS 주입한 마우스의 기도는 대조군과 달리 술잔세포와 섬모세포들을 관찰할 수 없이 점액이 꽉 채워져 있는 것으로 관찰되어진다. Cilia 또한 건강하게 보이지 못하고 점액과 다른 분비물이 붙어 있는 것으로 관찰되었다.
2. Activating G-protein Signaling(AGS) 3의 G-Protein Regulatory(GPR) Domain 연구
인간 호흡기에서 LPS, TNF, IL-1과 같은 염증성 인자에 의해 활성화된 백혈구에 의해 분비되는 C-X-C Motif Chemokine(CXCL) 12 [Stromal Cell-Derived Factor(SDF) 1]에 의해 호흡기 염증이 증가되는데 아직까지 기전이 정확하게 규명되어지지 않았다. 본 연구실에서는 CXCL12의 수용체이자 GPCR인 CXCR4 레벨에서 AGS3의 GPR Motif가 아주 중요한 기능함을 밝혔다. GPR Motif의 생화학적 기능은 Giα-GDP에 결합하여 이 결합을 안정화시키고, Heterotrimer인 Gαβγ의 결합을 억제하는 GDP Dissociation Inhibitor(GDI)로 작용한다 (그림 2). 이 연구의 중요성은 수용체의 신호를 Accessary G-Protein 단백질인 AGS3의 GPR Motif가 작용한다는 것을 증명하였으며, 이를 Peptide로 제작하여 마우스에 주입하였더니 CXCL12에 의한 염증이 효과적으로 억제함을 관찰하였다 (그림 3). 또한 CXCL12가 Chemokine이기 때문에 세포 표면에 있는 Actin의 재조합에도 GPR Motif Peptide가 효과적으로 억제함을 증명하여 호흡기 염증 치료약품 개발에 기조자료를 제시했다.
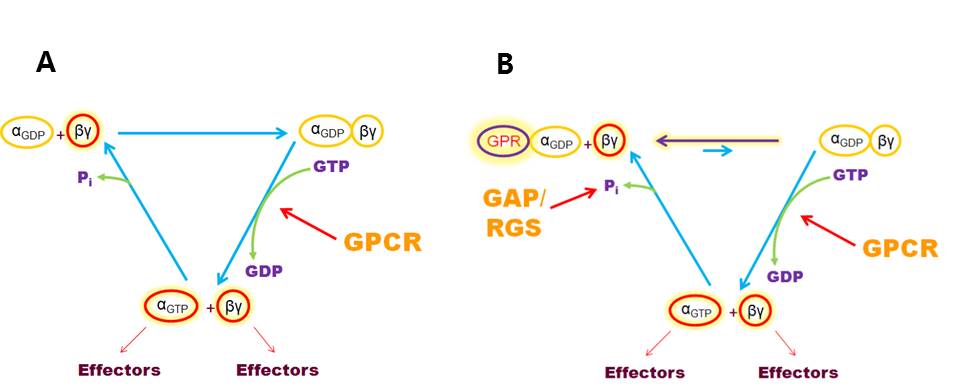
그림 2. 정상적인 G-Protein Cycle (A). G-Protein Cycle을 조절하는 RGS와 GPR 모식도 (B).
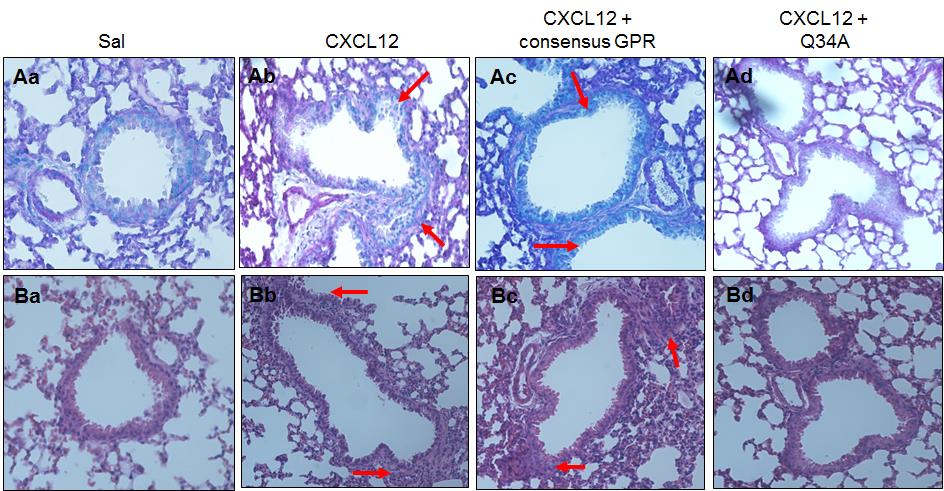
그림 3. GPR Peptide를 마우스에 주입 5일 후 희생시켜 폐 조직을 AB-PAS 염색법 (A)으로 염색하였더니 Ab처럼 염증성 세포가 증가하였지만, GPR Peptide를 주입하면 염증이 줄어드는 것을 관찰하였다 (Ad). 또한 H&E 염색 결과로 보면 CXCL12 처리 후 염증성 세포가 증가되었지만 (Bb), GPR Peptide를 주입하면 염증성 세포가 줄어드는 것을 관찰하였다 (Ad).
3. 미세먼지가 호흡기에 침윤되는 기전연구
미세먼지는 지름 2.5 μm 이하의 초미세먼지로 지름 4∼10 μm인 황사보다 크기가 훨씬 작다. 스모그 속 미세먼지는 지름 2.5 μm 이하의 초미세먼지로 특히 중국에선 겨울 난방용으로 사용되는 무연탄, 약 2억대의 자동차에서 황 함량이 높은 고농도 오염 물질을 배출하는 있는 것이 중국 스모그 발생원인으로 거론되고 있으며, 이러한 중국 스모그가 편서풍을 따라 한반도로 유입되어 발생한다. 미세먼지는 사람의 폐포까지 깊숙이 침투해 만성 기관지염, 폐기종, 비염 등 각종 호흡기 질환을 일으키는 것으로 알려져 있고, 면역력을 떨어뜨리고 신장이나 신경계에도 지대한 영향을 미친다 (그림 4).
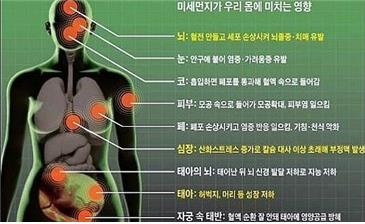
그림 4. 미세먼지가 인체에 미치는 영향
또한 호흡기뿐만 아니라 뇌졸중, 눈질환, 부정맥, 태아의 성장장애 등 인체의 많은 영향을 미친다. 본 연구실에서는 이러한 문제점을 해소하기 위하여 미세먼지의 침윤을 억제할 수 있는 밀착연접단백질의 발현을 조절하는 단백질의 규명하여 Peptide로 제작한 후 미세먼지의 침윤을 최소화시키는 물질을 개발하고 있다.
[연구책임자]

송경섭 교수
주소: 부산광역시 서구 감천로 262 고신대학교 의과대학 생리학교실
전화: 051-990-6236
팩스: 051-990-3081
E-mail: kssong@kosin.ac.kr
[연구진구성]

교수: 송경섭
포스트닥터: 박가영
조교: 오다교, 김연희
[대표논문]
1. Choi, I.H., Ahn, D.W., Choi, J.K., Cha, H.J., Ock, M.S., You, E., Rhee, S., Kim, K.C., Choi, Y.H., and Song, K.S.
(2016) Regulation of Airway Inflammation by G-protein Regulatory Motif Peptides of AGS3 protein. Sci Rep 6: 27054
2. Jeong, J.Y., Kim, J., Kim, B., Kim, J., Shin, Y., Kim, J., Ryu, S., Yang, Y.M. and Song, K.S. (2016) IL-1ra
secreted by ATP-induced P2Y2 regulates negatively MUC5AC overproduction during airway inflammation.
Mediat Inflamm 7984853.
3. Cha, H.J., Jung, M.S., Ahn, D.W., Choi, J.K., Ock, M.S., Kim, K.S., Yoon, J.H., Song, E.J., and Song, K.S. (2015)
Silencing of MUC8 by siRNA increases P2Y2-induced airway inflammation.
Am J Physiol Lung Cell Mol Physiol 308(6): L495-502.
4. Jeong, J.Y., Cha, H.J., and Song, K.S. (2014) ATP significantly increases P2Y2-dependent RANTES secretion
and overexpression in human airway epithelial cells. Genes Genom 36(5): 655-659.
5. Song, K.S., Choi, J.K., and Ahn, D.W. (2013) Src Homology 2-containing Protein Tyrosine Phosphatase (SHP-2) acts
as a negative regulator for MUC5AC transcription via the inhibition of the ERK1/2 MAPK signaling pathway in
the airway. Acta Physiol. 208 (3):245-250.
6. Kim, Y.S. and Song, K.S. (2013) Defective expression of Regulator of G-protein Signaling (RGS) 4 increases MUC5AC
overproduction in the epithelium of human nasal polyps. Tissue Eng Reg Med 10(1):33-37.
7. Song, K.S., Yoon, J.H., Kim, K.S., and Ahn, D.W. (2012) c-Ets1 inhibits the interaction of NF-κB and CREB and
down-regulates IL-1β-induced MUC5AC overproduction during airway inflammation. Mucosal Immunol. 5(2): 207-215.
8. Kim, Y.O., Jung, M.J., Choi, J.K., Ahn, D.W., and Song, K.S. (2011) Peptidoglycan from Staphylococcus aureus
increases MUC5AC gene expression via RSK1-CREB pathway in human airway epithelial cells.
Mol. Cells 32(4): 359-365.